Médicament : un anticoagulant est rappelé partout en France, en raison d’une « contamination croisée »
Posted 1 avril 2026 by: Admin
Les alertes sanitaires liées aux produits de consommation se multiplient, touchant parfois des médicaments largement utilisés.

Dernièrement, une communication officielle a signalé le retrait d’un anticoagulant distribué en France, en raison d’un défaut détecté lors de sa fabrication, suscitant une vigilance accrue des autorités sanitaires.
La plateforme RappelConso relaie régulièrement des retraits concernant divers produits, allant de l’alimentaire aux biens de consommation. Plus rarement, des médicaments sont concernés. C’est le cas du Rivaroxaban Viatris 20 mg, dont certaines boîtes ont récemment fait l’objet d’un rappel, selon une communication de l’ANSM datée du 25 mars 2026. La décision intervient à la suite de la détection d’un défaut de qualité sur un lot spécifique du médicament.
Un anticoagulant utilisé contre les caillots sanguins
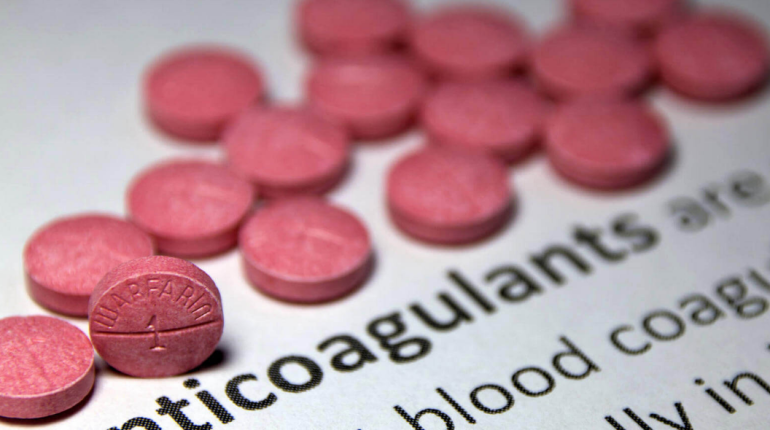
Le Rivaroxaban Viatris 20 mg est un traitement appartenant à la famille des anticoagulants. Il est prescrit pour prévenir et traiter la formation de caillots sanguins dans les vaisseaux, notamment dans certaines pathologies cardiovasculaires. Présenté sous forme de comprimé pelliculé, il est comparable, dans son enrobage, à d’autres médicaments courants tels que l’ibuprofène ou le tramadol. Ce traitement est fabriqué par Viatris Santé, filiale française du groupe Viatris, issu de la fusion entre Mylan et Upjohn (Pfizer).
Un lot précis identifié et concerné
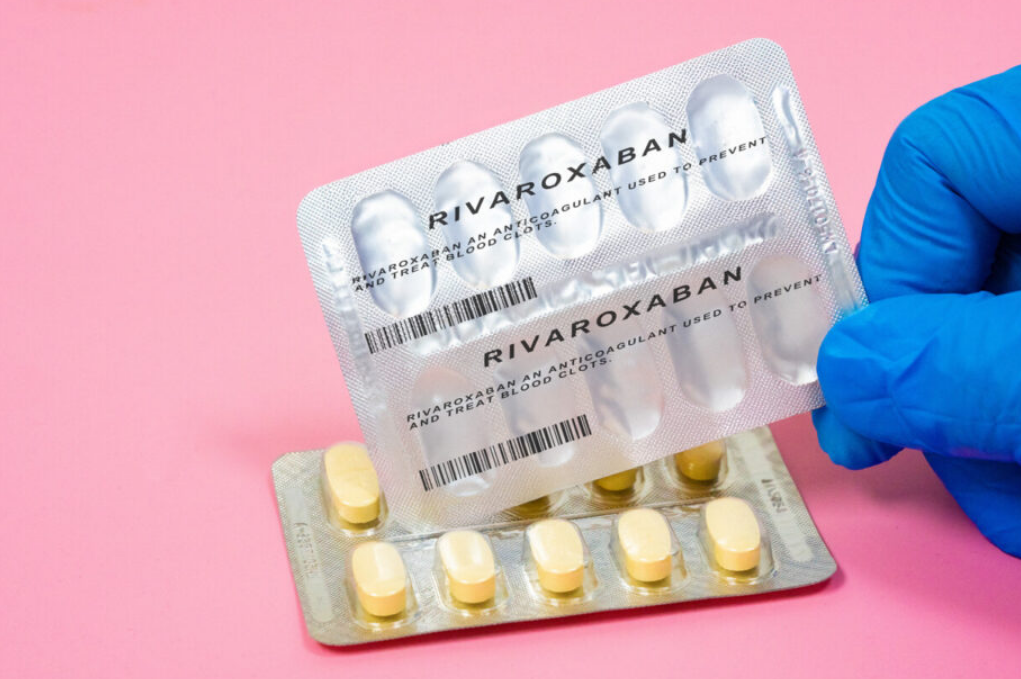
Les autorités sanitaires précisent que le rappel concerne uniquement le lot numéro 8212020, dont la date de péremption est fixée à juillet 2028. Ce signalement fait suite à une alerte transmise par le laboratoire lui-même, qui a identifié une anomalie lors du processus de fabrication. L’objectif de ce rappel est de retirer du circuit les boîtes potentiellement affectées afin de garantir la sécurité des patients.
Une contamination détectée lors de la fabrication
Selon les informations communiquées, le défaut constaté correspond à une contamination en très faible quantité par un autre médicament, la quétiapine. Cette substance, utilisée dans le traitement de certains troubles psychiatriques, aurait été introduite accidentellement lors de la production. Bien que les quantités évoquées soient minimes, les autorités appliquent un principe de précaution strict, justifiant le retrait immédiat du lot concerné.

















